Para mis estudiantes de 3* de Química/2013, les dejo una breve reseña de lo visto en el curso sobre el tema para ayudarles a imaginar el proyecto a presentar..
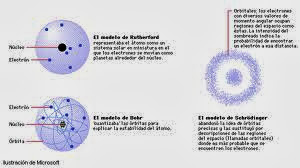
A través de la historia y siguiendo su trabajo experimental, su intuición y los trabajos de sus predecesores; los científicos fueron modificando los modelos atómicos para adecuarlos a lo que se observa en los fenómenos naturales y artificiales del avance de las ciencias en su conjunto.
Este proceso es de nunca acabar..en él se basa el avance de la Química como Ciencia..por eso es un MODELO..que nos representa y explica de la mejor manera lo que se observa y experimenta en cada tiempo..pero nunca es un MODELO ACABADO..siempre está en permanente CAMBIO.
 >> LOS MODELOS
>> LOS MODELOS
FUERON EVOLUCIONANDO SEGÚN:
MÁS DETALLADAMENTE>
LOS CIENTÍFICOS
Y SUS DESCUBRIMIENTOS
 MAPA CONCEPTUAL - ESQUEMA:
MAPA CONCEPTUAL - ESQUEMA:
NOTA> Para ver y ampliar las imágenes, selecciónalas y ábrelas en una ventana a parte donde podrás utilizar el "zoom".
# AQUÍ LES DEJO EL LINK PARA MIS ALUMNOS DE 3ro CON LOS TEMAS DE LAS EVALUACIONES FINALES SEGÚN LA CATEGORÍA (pueden descargarlos ya que están en formato word)
EVALUACIÓN CATEGORÍA "A" 2013
EVALUACIÓN CATEGORÍA "B" 2013
EVALUACIÓN CATEGORÍA "C" 2013

EVALUACIÓN CATEGORÍA "A" 2013
EVALUACIÓN CATEGORÍA "B" 2013
EVALUACIÓN CATEGORÍA "C" 2013

MUCHA SUERTE A TODOS!!!